Acalasia
Acalasia
El
término acalasia, proviene del griego "que no se relaja".
Obedece a un trastorno primario de la motilidad esófagica de etiología
desconocida, que resulta en disfagia ilógica, dolor torácico, mal nutrición y
baja ponderal. En ella existe una falla en la relajación e hipertensión del
esfínter esofágico inferior (EEI), junto con la alteración y pérdida progresiva
de la peristalsis. Es de baja ocurrencia y se estima, según datos
epidemiológicos norteamericanos, una prevalencia menor a 1/10.000 habitantes y
una incidencia estable del orden de 1,63/100.000, siendo la edad promedio de
diagnóstico cercana a los 53 años.1,2
Los
pacientes afectados conllevan además una reducción significativa de la
expectativa de vida y se asocia incluso a patología neoplásica maligna.
Fisiopatología
A
nivel histológico, diversos estudios han demostrado la degeneración y pérdida
neuronal del plexo mientérico (de Auerbach) a nivel esofágico distal, hallazgo
encontrado en >90% de los casos.
Esta
degeneración ocurre de manera selectiva, afectando predominantemente a neuronas
inhibitorias productoras de óxido nítrico, sin lesionar a neuronas
colinérgicas.1,3
Sin
embargo ésta denervación mientérica no ocurre exclusivamente en esófago, sino
que puede extenderse, en cerca de la mitad de los casos, hasta nivel del tercio
medio gástrico, sin afectar porciones intestinales.
Acalasia y cancer de esofago
La
acalasia es considerada al mismo tiempo una enfermedad premaligna. El riesgo
relativo de desarrollar cáncer esofágico de células escamosas varía enormemente
en publicaciones, siendo desde 0 a 140 veces respecto a la población normal,
esto incluso después de haber sido tratada quirúrgicamente. Estudios en
autopsias han reportado prevalencias de neoplasia esofágica de hasta 29% en
pacientes con acalasia.
La
causa exacta de esta asociación no es clara. Se ha propuesto a la fermentación
de comida retenida, el crecimiento bacteriano y la producción de nitrosaminas
como mecanismo causal, así como al reflujo gastroesofágico patológico posterior
a la resolución quirúrgica. Sin embargo, se desconoce si la acalasia determina
la aparición del cáncer o viceversa.
Clínica
El
síntoma principal es la disfagia, tanto para líquidos como para sólidos. Una
disfagia ilógica nos obliga a pensar en este diagnóstico. Otros síntomas
incluyen la dificultad para eliminar gases por boca, dolor torácico, pirosis y
regurgitación alimentaria, la que puede ser suficientemente severa como para
causar complicaciones pulmonares como tos o neumonia aspirativa. Se asocia
usualmente a baja ponderal.
Se ha
estudiado que entre el inicio de las manifestaciones sintomáticas y el
diagnóstico, existe habitualmente un retardo aproximado de 5 años.
Estudio
El
diagnóstico de acalasia se realiza en base a la sospecha clínica apoyado por la
manometría esofágica y la esofagografía baritada.
Siempre
debe excluirse la pseudo acalasia, diagnósticos diferenciales y posibles
complicaciones asociadas, donde la tomografía computada, la endosonografía y la
endoscopía juegan un rol fundamental.
Radiografía
simple
Estudio
no específico, aunque altamente disponible, que puede sugerir el diagnóstico
mediante detección de anomalías estructurales. Los principales hallazgos
compatibles son la presencia de ensanchamiento mediastínico secundario a
dilatación esofágica y la ausencia de burbuja gástrica.


Radiografía
contrastada
La
radiografía baritada, es capaz de evaluar estructural y funcionalmente el
esófago. Es el método de screening primario al enfrentar al paciente con
disfagia y se encuentra ampliamente disponible. Necesita de menor experiencia
que la manometría esofágica para interpretar resultados. Posee una
especificidad del 95% para el diagnóstico de acalasia.
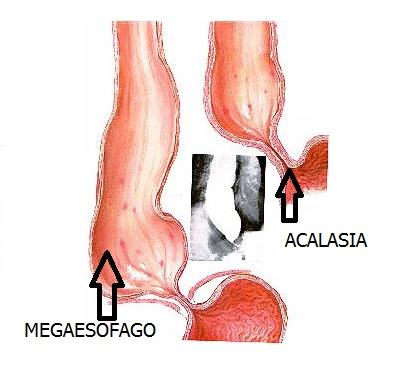
Los
hallazgos clásicos, son la presencia de dilatación esofágica e imagen en
"pico de pájaro", que hace referencia al estrechamiento progresivo
del lumen esofágico hacia distal y la forma característica que adopta el medio
contrastado retenido. Otros son la presencia de nivel hidroaéreo o tortuosidad
esofágicos distales.

Esta
herramienta diagnóstica permite además clasificar la progresión anátomo
radiológica según gravedad en:
•
|
Tipo
I Precoz: trastorno motor, sintomático, sin dilatación
esofágica.
|
•
|
Tipo
II No avanzado: con dilatación <10 cm (8 cm para algunos
autores)
|
•
|
Tipo
III Avanzado: con dilatación >10 cm
|
•
|
Tipo
IVA vanzado: con dilatación más de 10 cm y de tipo megaesófago
sigmoideo.13
|
Esta
clasificación presenta utilidad en el seguimiento y pronóstico de la patología,
al encontrarse estandarizado, ser de bajo costo y tener buena correlación con
resultados clínicos y manométricos.
Un
esófago <3 cm en diámetro, una columna de bario <1 cm después de 5
minutos de su ingesta y un diámetro de 8 a 10 mm de la unión esofago-gástrica
son criterios de buena respuesta a la terapia.14
Sin
embargo, su sensibilidad no es óptima, dado que un estudio sin hallazgos patológicos,
no permite descartar acalasia, especialmente en estadios tempranos de la
enfermedad. Esto, debido a que las alteraciones fisiopatológicas preceden al
desarrollo de los hallazgos anatómicos discernibles radiológicamente. Es en
este aspecto donde cobra mayor importancia la manometría esofágica.14
Manometría Esofágica
Es el
estándar de oro en el diagnóstico de acalasia esofágica. Los hallazgos
concordantes con el cuadro son la hipertonía del EII sobre 45 mmHg, la
relajación incompleta del EEI (normalmente bajo 8 mmHg), y la aperistalsis o
peristalsis inefectiva. Debido a su alta sensibilidad, es útil desde estados
iniciales de enfermedad.15
Manometría
Esofágica de alta resolución
Estudio
más especializado que utiliza 36 sensores dispuestos cada un centímetro.
Permite
evaluar con mayor detalle la variabilidad que existe en el peristaltismo
alterado entre los diferentes pacientes con acalasia, y clasificarlos en tres
subtipos según su comportamiento manométrico:
-
|
Tipo I o clásico: sin cambios en presiones
esofágicas, hipertonía EEI.
|
-
|
Tipo II: presurización simultánea a lo largo
del esófago.
|
-
|
Tipo III o espástica: presiones muy elevadas.
|
Su
relevancia radica en que puede predecir la probabilidad de una buena respuesta
terapéutica en general. (Tipo II 70-100%, Tipo I 50-73%, Tipo III 30%).10,16
Posterior
a la cirugía, una presión manométrica del EEI < 10 mmHg, es criterio de
buena respuesta a la terapia.
Tratamiento
El
objetivo del tratamiento es corregir la obstrucción funcional del EEI. Ninguna
terapia ha sido capaz de revertir la pérdida neuronal, de modo que debe
considerarse como paliativa o sintomática, de causa aún intratable.
Los
esfuerzos se dirigen a disminuir la presión del EEI para facilitar el
vaciamiento esofágico, mejorar los síntomas, y prevenir las complicaciones
relacionadas al éstasis y dilatación esofágicos progresivos, evitando además la
aparición de reflujo gastroesofágico posterior al tratamiento.
Las
modalidades terapéuticas consideran el tratamiento farmacológico,
procedimientos endoscópicos, y cirugía. No obstante, ninguno es capaz de
restaurar la peristalsis esofágica o la presión normal del EEI.
Farmacológico
El
tratamiento médico posee efecto limitado y transitorio. Puede ser clasificada
como sistémico o local.
Sistémico
Los
bloqueadores de canales de calcio, sildenafil e isosorbide han demostrado sólo
eficacia limitada, con efectos adversos en porcentajes inaceptables.10,13
Local
La
inyección endoscópica local en el EEI de toxina botulínica posee un potente
efecto inhibidor de la liberación de acetilcolina. Presenta resultados
excelentes en forma inmediata, con más de un 90% de respuesta satisfactoria.
Sin embargo la duración de ésta es limitada, en promedio 6-9 meses.
Las
complicaciones suelen ser muy infrecuentes, debido a que se utilizan dosis
bajas. Entre ellas destaca la fibrosis a largo plazo, y la posibilidad de
dificultar otras terapias. Su mayor utilidad sería en pacientes ancianos y de alto
riesgo quirúrgico.10,13,17,18
Endoscópico
La
dilatación endoscópica utiliza más frecuentemente al balón neumático Rigiflex,
y puede ser guiado tanto endoscópica como fluoroscópicamente. Posee diámetros
de 3,0; 3,5 y 4,0 cm, de uso secuencial según sea la respuesta clínica.
El
número de dilataciones y el tiempo requerido de inflado para una dilatación
exitosa varían y son operador dependientes. En general se recomienda cirugía
después de 3 dilataciones sucesivas ineficaces.
No
existe consenso en cuanto a la técnica a utilizar, la cual varía en diámetro de
balón a utilizar (2,5 a 5 cm), presión de insuflación (100 a 1000 mmHg), tiempo
de insuflación (seg a 5 min), y número de insuflaciones por sesión (1 a 5).
Las
principales complicaciones son perforación esofágica (2-6%), hematoma
intramural, divertículo cardial, desgarro de mucosa esofágica y reflujo
gastroesofágico (2%).
Representa
una técnica poco invasiva, utilizada de preferencia en muchos centros, pero la
alta probabilidad de reintervenciones y los riesgos asociados han puesto en
duda su costo-efectividad comparada a la miotomía.
Factores
de riesgo de fracaso de la técnica son:
-
|
Edad < 40-45 años.
|
-
|
Sexo masculino.
|
-
|
Dilatación única con balón de 3.0 cm.
|
-
|
EEI con presiones sobre 10-15 mmHg posterior a
procedimiento.
|
-
|
Pobre vaciamiento gástrico en radiografía
baritada.
|
-
|
Acalasia tipo I y III según manometría de alta
resolución.
|
Quirúrgico
-
|
Miotomía esofágica.
|
-
|
Funduplicatura
Bibliografía
“Cuadernos de ciruga (Valdivia) - Acalasia esofgica.” Revistas Electr, mingaonline.uach.cl/scielo.php?pid=S0718-28642012000100004&script=sci_arttext.
|
Comentarios
Publicar un comentario